«Η ογκολογία στο κομμάτι της έρευνας ζει μια πολύ μεγάλη επανάσταση με τις νέες τεχνικές στο εργαστήριο», αναφέρει στο ΒΗΜΑ η Μαριάννα Ραψομανίκη, επίκουρη καθηγήτρια στο Biomedical Data Science Center του Πανεπιστημιακού Νοσοκομείου της Λωζάνης και του Πανεπιστημίου της Λωζάνης, όπου και ηγείται της ερευνητικής ομάδας AI for Biomedicine.
Η έρευνα της ομάδας της Μαριάννας Ραψομανίκη επικεντρώνεται στην ανάπτυξη μεθόδων τεχνητής νοημοσύνης και μηχανικής μάθησης προσαρμοσμένων σε σύνθετα, πολυτροπικά βιοϊατρικά σύνολα δεδομένων, με στόχο την αποσαφήνιση των μηχανισμών του καρκίνου και της ετερογένειας των όγκων.
Μιλά στο ΒΗΜΑ για τις νέες εργαστηριακές τεχνικές που χρησιμοποιούνται στην ογκολογία, για τη συμβολή της τεχνητής νοημοσύνης στην έρευνα, για την πολυπλοκότητα της νόσου, αλλά και για τις ρεαλιστικές προσδοκίες που πρέπει να έχουμε όταν διαβάζουμε άρθρα με πηχυαίους τίτλους για τη θεραπεία του καρκίνου.
«Η αλήθεια είναι ότι γίνεται πολύ μεγάλη ερευνητική προσπάθεια και έχουν βελτιωθεί πολλά στη θεραπεία του καρκίνου τα τελευταία χρόνια, όμως οφείλουμε να βάζουμε τα πράγματα στη σωστή τους βάση. Ο καρκίνος εξακολουθεί να είναι μια πάρα πολύ δύσκολη νόσος, μια νόσος πολυπαραγοντική», επισημαίνει η κα Ραψομανίκη.
Και συμπληρώνει κατευθείαν, θέλοντας να προλάβει τυχόν υπερβολικούς τίτλους και παραμένοντας προσηλωμένη στο έργο της. «Η έρευνα δεν είναι τι κάνω εγώ και τι κάνει κάποιος άλλος. Έρευνα είναι τι κάνουμε όλοι μαζί».
Δηλώνει αισιόδοξη για τη θεραπεία του καρκίνου του μαστού και βέβαιη ότι η τεχνητή νοημοσύνη σίγουρα δεν θα αντικαταστήσει -και δεν θα έπρεπε- τους γιατρούς.
Θα ξεκινήσω με την ερώτηση που διατυπώνεται πιο συχνά από καμία άλλη: γιατί δεν έχουμε ακόμα θεραπεύσει τον καρκίνο;
Από την αρχή των σπουδών μου ασχολούμαι με την Ογκολογία. Όσο πιο πολλά μαθαίνω τόσο πιο πολύ καταλαβαίνω γιατί είναι τόσο δύσκολο να δοθεί αυτή η απάντηση.
Η πολυπλοκότητα αυτής της νόσου είναι πραγματικά γιγάντια. Είναι μια πολύ χαοτική και πολυπαραγοντική νόσος. Είναι το περιβάλλον. Είναι το γενετικό υπόβαθρο.
Είναι πολλά που μπαίνουν στην εξίσωση. Ο καρκίνος δεν είναι μία νόσος, αλλά εκατοντάδες νόσοι σε μία. Ακόμα κι αν μιλάμε για τον ίδιο καρκίνο, για παράδειγμα τον καρκίνο του μαστού, δεν είναι ο ίδιος καρκίνος σε όλες τις γυναίκες.
Τα τελευταία δέκα χρόνια έχει επέλθει μια ερευνητική επανάσταση. Έχουμε νέους τρόπους να αναλύουμε τους καρκινικούς όγκους και να παίρνουμε δεδομένα από αυτούς.
Έχουμε νέους αλγορίθμους για να αναλύουμε αυτά τα δεδομένα με τη βοήθεια της τεχνητής νοημοσύνης.
Σε επίπεδο έρευνας, πού βρισκόμαστε αυτή τη στιγμή;
Η μεγάλη πρόκληση στην έρευνα ενάντια στον καρκίνο είναι η ετερογένεια της νόσου. Κάθε όγκος είναι ένα μοναδικό οικοσύστημα.
Μπορούμε να το σκεφτούμε με αναλογία ενός πραγματικού οικοσυστήματος στη φύση. Κάπως έτσι είναι οργανωμένος κι ένας όγκος, από την άποψη ότι έχουμε διαφορετικών ειδών καρκινικά κύτταρα που έχουν μεγάλη διαφορά γονιδιακά: τι είναι δηλαδή το DNA τους; γιατί τα καρκινικά κύτταρα πολλαπλασιάζονται πολύ γρήγορα και αποκτούν πολύ γρήγορα μεταλλάξεις;
Πρόκειται για ένα δυναμικό και σύνθετο οικοσύστημα. Από την άλλη έχουμε κύτταρα του «μικροπεριβάλλοντος» τα οποία είναι κύτταρα του ανοσοποιητικού ή άλλου είδους κύτταρα που περιβάλλουν τον όγκο.
Η αλληλεπίδραση των καρκινικών κυττάρων με τα κύτταρα του μικροπεριβάλλοντος είναι αυτή τη στιγμή το επίκεντρο της έρευνας στην ογκολογία.
Επομένως, η έρευνα έχει επικεντρωθεί στην κατανόηση της αλληλεπίδρασης των διαφορετικών κυττάρων μέσα σε ένα οικοσύστημα;
Ακριβώς. Μια τυπική θεραπεία είναι η ανοσοθεραπεία που πάει και επεμβαίνει σε αυτές τις αλληλεπιδράσεις. Τα τελευταία χρόνια η ανοσοθεραπεία έχει φέρει επανάσταση στη θεραπεία του καρκίνου.
Αυτό που δεν ξέρουμε όμως είναι ποιοι ασθενείς επωφελούνται από την ανοσοθεραπεία, ποιοι είναι οι καλοί υποψήφιοι. Είναι πολλές οι φορές που βλέπουμε ότι υπάρχει μεγάλη διαφορά στην απόκριση στην ανοσοθεραπεία σε διαφορετικούς ασθενείς.
Το γιατί κάποιοι επωφελούνται και κάποιοι όχι, δεν το ξέρουμε ή μάλλον δεν το ξέρουμε καλά. Επίσης δεν ξέρουμε γιατί κάποια είδη καρκίνου αντιδρούν καλύτερα στην ανοσοθεραπεία, ενώ κάποια άλλα όχι.
Όλα αυτά έχουν να κάνουν με το πώς είναι οργανωμένα τα κύτταρα στον χώρο. Αυτό ακριβώς κάνουμε εμείς στο εργαστήριό μου: έχουμε επικεντρωθεί στο να μοντελοποιήσουμε έναν όγκο, τον οποίο μπορούμε να σκεφτούμε ως ένα τεράστιο δίκτυο συνδέσεων.
Τα μοντέλα αυτά που προσπαθούμε να δημιουργήσουμε μπορούν να καταλάβουν καλύτερα πώς αλληλεπιδρούν τα κύτταρα μεταξύ τους μέσα σε έναν όγκο κι αν τους χορηγήσουμε διαφορετικά φάρμακα τι θα αλλάξει.
Μπορείτε να μας εξηγήσετε ποιες νέες εργαστηριακές τεχνικές χρησιμοποιούνται στην ογκολογία, όπως οι multiplexed imaging και spatial transcriptomics;
Τα τελευταία χρόνια έχουμε δει να συντελείται επανάσταση από κάποιες πειραματικές τεχνικές στο εργαστήριο, οι οποίες έχουν αλλάξει απόλυτα το πώς αντιμετωπίζουμε παγκοσμίως την έρευνα στον καρκίνο.
Οι καινούργιες αυτές τεχνικές μάς επιτρέπουν να μετρήσουμε ένα προς ένα τα κύτταρα μέσα στον καρκινικό όγκο. Κυριολεκτικά μπορούμε να απομονώσουμε τα κύτταρα και να μετρήσουμε μέσα σε κάθε μοναδικό κύτταρο τι συμβαίνει, ποια γονίδια μεταγράφονται, πόσο mRNA υπάρχει, από ποια γονίδια, ποιες πρωτεΐνες.
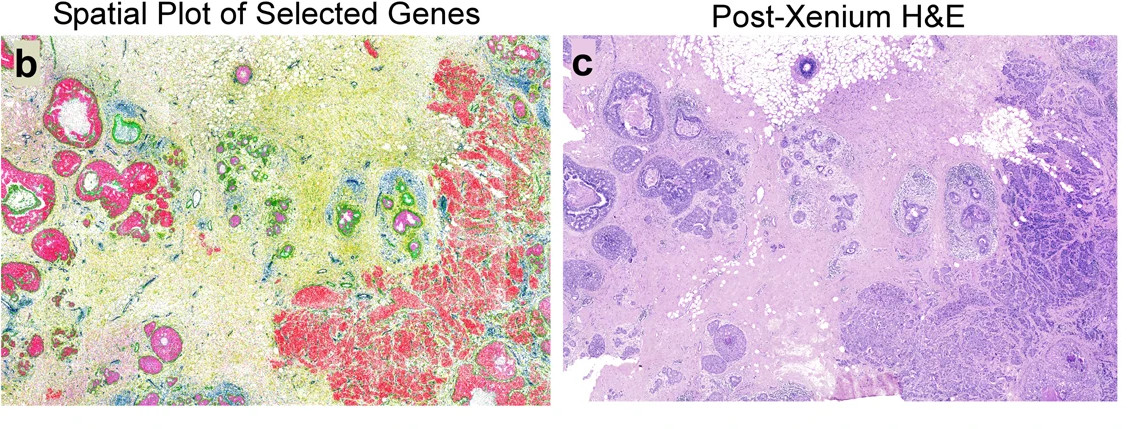
Ένα παράδειγμα για την εργαστηριακή τεχνική spatial transcriptomics: Βλέπουμε μια βιοψία ενός όγκου το μαστού (δεξιά) και στα αριστερά με διαφορετικά χρώματα βλέπομε ακριβώς ποια γονίδια μεταγράφονται στα κύτταρα αυτά. (πηγή: δημοσίευση)
Όταν ξεκίνησα εγώ το διδακτορικό μου είχαν κυκλοφορήσει οι πρώτες δημοσιεύσεις που μπορούσαν να το πετύχουν αυτό για πολύ λίγα κύτταρα. Τώρα το κάνουμε για εκατοντάδες ασθενείς, σε εκατομμύρια κύτταρα.
Αυτό βοηθάει και στο είδος της θεραπείας που θα επιλεχθεί, σωστά;
Φυσικά, γιατί έχεις μια πλήρη εικόνα για το τι κύτταρα υπάρχουν σε κάθε ασθενή και ανάλογα με αυτή την πλήρη εικόνα μπορείς να καταλάβεις πώς υποομαδοποιείται ο συγκεκριμένος όγκος: δηλαδή έχει πολλά κύτταρα του ανοσοποιητικού ή δεν έχει καθόλου και πού βρίσκονται σε σχέση με τα καρκινικά.
Τα καρκινικά που έχει τι είδους είναι, τι μεταλλάξεις έχουν; Αυτή ήταν και η δημοσίευση που κάναμε το 2019 για τον καρκίνο του μαστού, μια ερευνητική συνεργασία του Πανεπιστημίου της Ζυρίχης και του τμήματος Έρευνας της εταιρείας IBM.
Δημιουργήσαμε έναν «Άτλαντα» (breast cancer atlas) και μπορέσαμε να χαρτογραφήσουμε -σε επίπεδο μοναδικού όγκου και μοναδικού κυττάρου μέσα στον όγκο- πώς διαφέρουν οι όγκοι του καρκίνου του μαστού μεταξύ τους.
Μεταξύ άλλων, είδαμε ότι κάποιες ασθενείς σε πολύ προχωρημένο στάδιο είχαν έναν κλώνο καρκινικό αλλά πολύ επιθετικό, ενώ κάποιες άλλες μπορεί να είχαν πολλούς διαφορετικούς υποπληθυσμούς ταυτόχρονα, αλλά αυτό δεν τους έκανε επιθετικούς.
Η δημοσίευση αυτή είναι πάρα πολύ μεγάλη και θεωρείται μία από τις πιο επιδραστικές στον χώρο. Έχουν «χτίσει» πάνω σε όσα κάναμε.
Έγινε εφικτό χάρη στη συνεισφορά της τεχνητής νοημοσύνης;
Έγινε δυνατό επειδή μπορούσαμε να χρησιμοποιήσουμε αυτά τα νέα πειράματα και να πάρουμε τον όγκο πληροφορίας που μέχρι πρόσφατα δεν μπορούσαμε.
Μέχρι πρόσφατα για να αναλυθεί ένας όγκος σε επίπεδο ερευνητικό παίρναμε μια μέτρηση για να καταλάβουμε το προφίλ του. Τώρα μπορούμε να το κάνουμε αυτό σε επίπεδο μοναδικού κυττάρου, το οποίο είναι ουσιαστικά εκατομμύρια μετρήσεις για τον ίδιο όγκο.
Ο όγκος της πληροφορίας που παίρνουμε είναι τόσο μεγάλος που είναι αδύνατο να τον επεξεργαστούμε με απλά μαθηματικά.
Χρειάζονται μοντέλα, αλγόριθμοι και τεχνικές οι οποίες είναι φτιαγμένες ακριβώς για να μπορούν να μαθαίνουν από γιγάντια σύνολα δεδομένων.
Μπαίνουμε στον τομέα της μηχανικής μάθησης που πολλές φορές αναφέρεται ως τεχνητή νοημοσύνη. Το βασικό που πρέπει να έχουμε στο μυαλό μας είναι ότι η τεχνητή νοημοσύνη είναι ένας υπολογιστικά πιο εξελιγμένος τρόπος για να επεξεργαστούμε τη μαζική πληροφορία και να τη «διαβάσουμε».
Η τεχνητή νοημοσύνη συγκρίνει σε πολλές διαστάσεις ταυτόχρονα;
Δεν είναι ένα μοντέλο που θα σου πει στον εκάστοτε ερευνητή «κάνε αυτό». Ουσιαστικά θα του υποδείξει ποιες είναι οι σημαντικές διαφορές επειδή έχει την ικανότητα να συμπιέζει αποδοτικά την πληροφορία και να τη συγκρίνει σε πολλές διαστάσεις ταυτόχρονα.
Νομίζω πως μόλις απαντήσατε και στο αν η τεχνητή νοημοσύνη θα αντικαταστήσει τους ανθρώπους (ερευνητές, γιατρούς).
Η τεχνητή νοημοσύνη ναι μεν έρχεται να αλλάξει πάρα πολύ το πώς αντιμετωπίζουμε την έρευνα και την κλινική εφαρμογή σε διαφορετικά είδη καρκίνου -και όχι μόνο- αλλά ο ανθρώπινος παράγοντας της επαλήθευσης και της διεξαγωγής νέων πειραμάτων και το τι μπορεί να σημαίνει το κάθε τι το οποίο ένας αλγόριθμος προτείνει δεν μπορεί να παρακαμφθεί.
Η τεχνητή νοημοσύνη σίγουρα δεν θα αντικαταστήσει τους γιατρούς – και δεν πρέπει κατά την άποψή μου. Πάντα πρέπει να υπάρχει επαλήθευση, τόσο σε επίπεδο έρευνας όσο και σε επίπεδο κλινικής εφαρμογής.
Η τεχνητή νοημοσύνη μάς δίνει τη δυνατότητα να εξάγουμε υποθέσεις. Να κάνουμε προσομοιώσεις στον υπολογιστή εκατομμύρια φορές ώστε στη συνέχεια να μας βοηθήσει να επιλέξουμε τι πραγματικά πρέπει να δοκιμάσουμε στο εργαστήριο.
Ένας τρόπος να φιλτράρουμε την πληροφορία ή να βάλουμε σε προτεραιότητα τα πιο σημαντικά πράγματα που πρέπει να κάνουμε στο εργαστήριο. Κι αυτό έχει τεράστια αξία.
Σε σχέση με τον καρκίνο του μαστού πού βρισκόμαστε; Είστε αισιόδοξη;
Εγώ είμαι πάρα πολύ αισιόδοξη. Νομίζω ότι είναι θέμα χρόνου, ακριβώς γιατί πλέον έχουμε τη δυνατότητα να κοιτάξουμε μέσα στην πολυπλοκότητα του καρκίνου, με πολύ καλύτερα εργαλεία στα χέρια μας, με πολύ καλύτερα όπλα.
Θα μπορούμε να διαλέξουμε την καλύτερη θεραπεία για τον κάθε ασθενή, αυτό που λέμε δηλαδή εξατομικευμένη ιατρική. Αντί να παίρνουν όλοι οι άνθρωποι την ίδια θεραπεία, να είναι πιο στοχευμένη η θεραπεία στον κάθε ασθενή, στον κάθε όγκο μοναδικά.
Είμαι πολύ αισιόδοξη ότι στα επόμενα δέκα χρόνια θα δούμε τεράστιες αλλαγές, μεγάλη πρόοδο και θα αρχίσει σιγά σιγά να εφαρμόζεται και στην κλινική πράξη.
Καμιά φορά σκέφτομαι κιόλας ότι οι μελλοντικοί άνθρωποι θα βλέπουν πώς αντιμετωπίζουμε τον καρκίνο σήμερα και θα το βρίσκουν πολύ πρωτόγονο σε σχέση με το τι θα γίνεται στο μέλλον.
Όπως εμείς βρίσκουμε πολύ πρωτόγονο τον τρόπο αντιμετώπισης άλλων μολυσματικών ασθενειών, πριν τα εμβόλια, πριν τα αντιβιοτικά.
Μαρία Πολύζου: «Για μένα ο καρκίνος ήταν ευλογημένο δώρο»
Μιλάτε για βάθος δεκαετίας.
Κυριολεκτικά κάθε μέρα που ξυπνάω διαβάζω για καινούργιες σπουδαίες δημοσιεύσεις για διαφορετικά είδη καρκίνου. Ειδικά ότι έχει να κάνει με την ανοσοθεραπεία.
Στο Πανεπιστημιακό Νοσοκομείο της Λωζάνης υπάρχουν πάρα πολλοί άνθρωποι που δουλεύουν σκληρά γι’ αυτό.

Η Μαριάννα Ραψομανίκη με την ομάδα του εργαστηρίου. Από αριστερά: Marianna Rapsomaniki, Theo Maffei, Adriano Martinelli, Sari Issa, Melissa Ensmenger, Louie McConnel, Jieran Sun.
Από τη μία έχουμε έναν καλώς εννοούμενο ανταγωνισμό στον ακαδημαϊκό τομέα: σου δημιουργείται ένα άγχος ότι αυτό που κάνεις εσύ το κάνει και κάποιος άλλος και πρέπει να προλάβεις να δημοσιεύσεις, από την άλλη είναι πολύ ωραίο γιατί δείχνει ότι υπάρχει μια πολύ έντονη ερευνητική δραστηριότητα.
Η ογκολογία τα τελευταία χρόνια ζει μια μεγάλη ερευνητική επανάσταση και πιστεύω ότι είναι απλά θέμα χρόνου αυτό να μετουσιωθεί και κλινικά.
Είναι σημαντικό να βάζουμε τα δεδομένα στη σωστή βάση και να μην δημιουργούνται ψεύτικες ελπίδες.
Πάρα πολύ σημαντικό. Δεν θέλω να πιστεύει κάποιος ότι εμείς βγάλαμε μια δημοσίευση κι αυτό σημαίνει ότι θεραπεύσαμε τον καρκίνο. Δεν είναι έτσι.
Η πραγματικότητα είναι πολύ πιο σύνθετη και πρέπει να είναι σύνθετη πριν φτάσει οτιδήποτε στον ασθενή. Πρέπει να υπάρχει επαλήθευση.
Από τη μία θέλω να είναι ρεαλιστικές οι προσδοκίες που έχουμε όταν διαβάζουμε άρθρα «επιστήμονες βρήκαν κάτι ή σπουδαία δημοσίευση για τον καρκίνο» γιατί ο κόσμος νομίζει ότι τον κοροϊδεύουμε και τίποτα δεν έχει αλλάξει.
Από την άλλη δεν μπορώ να μην τονίσω ότι υπάρχει τεράστια ελπίδα σε όλη αυτή τη συντονισμένη προσπάθεια που γίνεται. Απλά πρέπει να την τοποθετούμε διαρκώς σε βάσεις ρεαλιστικές.
Ένα μεγάλο κομμάτι της αισιοδοξίας έγκειται και στο ότι νέοι άνθρωποι ασχολούνται πολύ παθιασμένα με αυτόν τον τομέα της έρευνας.