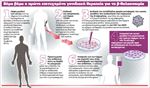
Από τα τρία χρόνια του η ζωή του εξαρτιόταν από μεταγγίσεις αίματος, απαραίτητες προκειμένου να ελέγχεται κατά το δυνατόν η άκρως σοβαρή μορφή θαλασσαιμίας από την οποία έπασχε. Επρόκειτο για την αποκαλούμενη Ε-β/0-β μορφή της νόσου, η οποία «πλήττει» κυρίως τους πληθυσμούς της Νοτιοανατολικής Ασίας- εκείνος, αν και γεννήθηκε στη Γαλλία, κρατούσε τη μισή καταγωγή του από την Ταϊλάνδη και την άλλη μισή από το Βιετνάμ. Είχε φθάσει πλέον 18 ετών, σε μια ηλικία που όλοι οι νέοι ονειρεύονται να ανοίξουν τα φτερά τους και να πετάξουν· τα δικά του τα φτερά όμως είχαν κοπεί, ενώ υπήρχε κίνδυνος να κοπεί ακόμη και το νήμα της ζωής του, αφού είχε φθάσει πια σε οριακό σημείο εξαιτίας της νόσου του αλλά και των παρενεργειών των μεταγγίσεων. Η προοπτική μιας μεταμόσχευσης μυελού των οστών δότη δεν ήταν δυνατή, αφού δότης συμβατός δεν υπήρχε. Και τα χρονικά περιθώρια στένευαν. Τότε μια μεγάλη ομάδα γιατρών από διαφορετικά κέντρα της Γαλλίας με επικεφαλής τον Φιλίπ Λεμπούλς, διευθυντή του Ινστιτούτου Αναδυόμενων Ασθενειών και Καινοτόμων Θεραπειών της γαλλικής Επιτροπής Ατομικής Ενέργειας (CΕΑ), καθηγητή στο Εθνικό Ινστιτούτο Υγείας και Ιατρικής Ερευνας (ΙΝSΕRΜ) και επισκέπτη καθηγητή στο Πανεπιστήμιο του Χάρβαρντ, χάρισε νέα φτερά στον 18χρονο ασθενή. Οι γιατροί εφήρμοσαν στον νεαρό για πρώτη φορά παγκοσμίως γονιδιακή θεραπεία ενάντια στη β-θαλασσαιμία, μια ασθένεια «συνυφασμένη» με το ελληνικό DΝΑεκτιμάται ότι ένας στους 12 Ελληνες και Ελληνίδες είναι φορέας της νόσου, γεγονός που μεταφράζεται σε κίνδυνο να φέρει στον κόσμο παιδιά με θαλασσαιμία σε περίπτωση που και ο/η σύντροφος είναι φορέας του ελαττωματικού γονιδίου που την προκαλεί (ο κίνδυνος όταν και οι δύο γονείς αποτελούν φορείς είναι της τάξεως του 25% για κάθε εγκυμοσύνη).
Η περίπτωση αυτού του ασθενούς, ο οποίος είναι πλέον 21 ετών, δημοσιεύθηκε πριν από περίπου έναν μήνα στην έγκριτη επιθεώρηση «Νature». Και όπως όλα δείχνουν, πρόκειται για μια πρωτιά που θα έχει αισιόδοξη συνέχεια, σύμφωνα με τα όσα είπε ο καθηγητής Λεμπούλς στο «Βήμα». Δεν είναι τυχαίο ότι τρία χρόνια μετά τη διεξαγωγή της διαδικασίας, ο μικρός ήρωας της ιστορίας μας, αλλά και της ιστορίας πολλών ανθρώπων με θαλασσαιμία, όχι μόνο ζει απαλλαγμένος από τις μεταγγίσεις αίματος αλλά έχει κατακτήσει το δικαίωμα σε μια ζωή με ποιότητα, κάνοντας όλα αυτά που θεωρούνται δεδομένα για την ηλικία του, όπως το να εργάζεται: συγκεκριμένα δουλεύει ως μάγειρας σε ένα εστιατόριο του Παρισιού. Σίγουρα θα μαγειρεύει ωραία φαγητά, ευχαριστώντας την επιστήμη και τους γιατρούς που «μαγείρεψαν» για εκείνον ένα καλύτερο μέλλον, ακολουθώντας μάλιστα μια εντελώς… νέα συνταγή για τη θαλασσαιμία. Οπως αποδείχθηκε, η συνταγή δεν έτυχε, πέτυχε!
Από σαράντα κύματα…
Η χρήση γονιδιακής θεραπείας για την αντιμετώπιση των αιμοσφαιρινοπαθειών αποτελούσε ένα στοίχημα ζωής για τον καθηγητή Λεμπούλς. Γενικώς, η γονιδιακή θεραπεία, πίσω από την οποία κρύβεται έρευνα τριάντα ολόκληρων χρόνων, έχει περάσει από σαράντα κύματα. Θεωρήθηκε αρχικώς λύση απέναντι σε πολλές κληρονομικές ασθένειες όταν άρχισαν να ανακαλύπτονται τα πρώτα γονίδια που συνδέονταν με αυτές. Ωστόσο οι πρώτες δοκιμές απογοήτευσαν τους επιστήμονες, αφού εμφανίστηκαν σοβαρές παρενέργειες, ενώ κατεγράφη ακόμη και θάνατος ασθενούς.
Συγκεκριμένα το 1999 ένας 18χρονος ο οποίος συμμετείχε σε δοκιμή γονιδιακής θεραπείας για την αντιμετώπιση μιας σπάνιας μεταβολικής διαταραχής πέθανε εξαιτίας πολυοργανικής ανεπάρκειας τέσσερις ημέρες μετά την έναρξη της θεραπείας. Ο θάνατός του πιστεύεται ότι προήλθε λόγω της εμφάνισης πολύ έντονης ανοσολογικής απόκρισης στον αδενοϊό που χρησιμοποιήθηκε ως φορέας μεταφοράς του κατάλληλου για την αντιμετώπιση της νόσου υγιούς γονιδίου στον οργανισμό του. Λίγα χρόνια μετά δύο παιδιά που έπασχαν από το σχετιζόμενο με το χρωμόσωμα Χ σύνδρομο σοβαρής συνδυασμένης ανοσοανεπάρκειας (Χ-SCΙD- γενετικό νόσημα κατά το οποίο δεν αναπτύσσεται το ανοσοποιητικό σύστημα, με αποτέλεσμα οι ασθενείς να ζουν σε ένα πλήρως αποστειρωμένο περιβάλλον) παρουσίασαν λευχαιμία ύστερα από εφαρμογή γονιδιακής θεραπείας.
Οι απογοητεύσεις αυτές δεν πτόησαν τον δρα Λεμπούλς, όπως ο ίδιος λέει. «Ακόμη και αν υπήρξαν σοβαρά προβλήματα,πρέπει να λάβουμε υπόψη μας ότι όλοι οι ασθενείς που συμμετείχαν σε τέτοιου είδους δοκιμές θα ήταν σήμερα νεκροί εξαιτίας της νόσου τους.Και όμως,οι περισσότεροι από αυτούς συνεχίζουν να ζουν, και μάλιστα μια φυσιολογική ζωή,χάρη στη γονιδιακή θεραπεία».
Το σωστό «εργαλείο»
Αυτή η πίστη του καθηγητή στις δυνατότητες της γονιδιακής θεραπείας τού χάρισε και την επιτυχία στο δύσβατο πεδίο. Εκείνος και η ομάδα του κρατούν τα πρωτεία της εφαρμογής επιτυχημένης γονιδιακής θεραπείας σε ποντίκια με δρεπανοκυτταρική αναιμία πριν από μία δεκαετία. Από τα ποντίκια ως τον άνθρωπο απαιτήθηκε όμως σκληρή δουλειά, η οποία, όπως είχαν δείξει οι προηγούμενες αποτυχίες, ήταν απαραίτητο να επικεντρωθεί στον κατάλληλο ιό-«όχημα» του γονιδίου στα κύτταρα του ασθενούς. Μέσα από συντονισμένες προσπάθειες διαφορετικών κέντρων αποδείχθηκε τελικώς ότι το κατάλληλο εργαλείο ήταν ο ιός ΗΙV του ΑΙDS (!). Μην τρομάζετε: επρόκειτο για μια τροποποιημένη, αδρανοποιημένη μορφή του ιού, η οποία δεν μπορεί να προκαλέσει πρόβλημα στον ανθρώπινο οργανισμό. Ο συγκεκριμένος ιός έχει το πλεονέκτημα ότι μπορεί να μεταφέρει μεγάλα τμήματα DΝΑ, γεγονός άκρως σημαντικό, αφού το γονίδιο της β-σφαιρίνης που παρουσιάζει ελάττωμα στη β-θαλασσαιμία έχει μεγάλο μέγεθος. Η β-σφαιρίνη είναι μια πρωτεΐνη που παίζει σημαντικό ρόλο στη σύνθεση της αιμοσφαιρίνης η οποία μεταφέρει το οξυγόνο από τους πνεύμονες στους ιστούς του σώματος. Η επιλογή αποδείχθηκε σωστή: χάρη στον ιό του ΑΙDS, ένας άνθρωπος που βρισκόταν στα πρόθυρα του θανάτου «ξαναγεννήθηκε».
Στη μορφή θαλασσαιμίας από την οποία έπασχε ο νεαρός ένα αντίγραφο του γονιδίου της β-σφαιρίνης δεν εκφράζεται καθόλου, ενώ το δεύτερο αντίγραφο εκφράζει σε πολύ χαμηλό ποσοστό μια μεταλλαγμένη μορφή της πρωτεΐνης (κληρονομούμε δύο αντίγραφα του κάθε γονιδίου, ένα από κάθε γονέα). Το αποτέλεσμα ήταν η εκδήλωση πολύ βαριάς αναιμίας και η συνεχής ανάγκη για μεταγγίσεις, οι οποίες συνδέονται με ποικίλες παρενέργειες. Ο 18χρονος αναγκάστηκε επίσης να υποβληθεί σε σπληνεκτομή, όπως συμβαίνει συχνά σε ασθενείς με θαλασσαιμία, αφού ο σπλήνας του διογκώθηκε εξαιτίας του συνεχούς «φιλτραρίσματος» παθολογικών ερυθρών αιμοσφαιρίων. Ελλείψει συμβατού δότη για μεταμόσχευση μυελού των οστών και με δεδομένο ότι η κατάστασή του είχε επιδεινωθεί σημαντικά, οι γιατροί προχώρησαν, αφού επιβεβαιώθηκαν ότι πληρούνται οι προϋποθέσεις εφαρμογής γονιδιακής θεραπείας, στη μεταμόσχευση των ίδιων των τροποποιημένων κυττάρων του. Αν η μέθοδος ήταν επιτυχημένη, θα είχε και ένα επιπλέον πλεονέκτημα: δεν θα υπήρχε κίνδυνος απόρριψης του μοσχεύματος.
Η διαδικασία
Ιδού η διαδικασία που ακολουθήθηκε διά στόματος του δρος Λεμπούλς: «Το υγιές γονίδιο που έπρεπε να εισαγάγουμε είναι αυτό που κωδικοποιεί την παραγωγή της β-σφαιρίνης. Ωστόσο τροποποιήσαμε ελαφρώς το γονίδιο- για την ακρίβεια,ένα αμινοξύ του- προκειμένου να έχουμε εικόνα της έκφρασής του μετά την εισαγωγή του στα κύτταρα (έναν δείκτη με λίγα λόγια που να απεικονίζει το εύρος της έκφρασής του στον οργανισμό).Στη συνέχεια λάβαμε κύτταρα του μυελού των οστών του ασθενούς τα οποία περιέχουν τα βλαστικά κύτταρα του αίματος. Εκθέσαμε τα κύτταρα για λίγες ώρες στον ιό-φορέα στο εργαστήριο προκειμένου να τα μολύνει και να εισαχθεί εντός τους το υγιές γονίδιο και ακολούθως τα καταψύξαμε».
Ενόσω οι ερευνητές ετοίμαζαν τα κύτταρα για την έγχυση πίσω στον οργανισμό, ο ασθενής εισήχθη στο νοσοκομείο και επί λίγες ημέρες υπεβλήθη σε ένα χημειοθεραπευτικό σχήμα, ώστε να κατασταλούν όλα τα «ελαττωματικά» κύτταρά του. Οταν ήταν έτοιμος, τα «νέα» κύτταρα εργαστηρίου αποψύχθηκαν και εισήχθησαν στην κυκλοφορία του αίματος, ακριβώς όπως όταν γίνεται μετάγγιση αίματος. «Μέσα σε λίγες ημέρες είχαν μεταναστεύσει στα οστά, αλλά απαιτήθηκαν κάποιες εβδομάδες προκειμένου να αρχίσει να λειτουργεί κανονικά ο νέος “επιδιορθωμένος” μυελός των οστών» σημειώνει ο καθηγητής Λεμπούλς. Ο ασθενής παρέμεινε στο νοσοκομείο για περίπου έναν μήνα, αλλά χρειάστηκε ένας χρόνος προκειμένου να απαλλαγεί πλήρως από τις μεταγγίσεις.
Χωρίς παρενέργειες
Στο κρίσιμο ερώτημα σχετικά με την εμφάνιση παρενεργειών από τη διαδικασία ο καθηγητής απαντά… σχεδόν αρνητικά. «Δεν έχουν παρατηρηθεί παρενέργειες σε κλινικό επίπεδο.Από την ανάλυση ωστόσο των περιοχών των χρωμοσωμάτων στις οποίες ενσωματώθηκε ο ιός-φορέας που μετέφερε το γονίδιο εντός των κυττάρων,προέκυψε ότι μια περιοχή εμφανιζόταν συχνότερα σε σύγκριση με τις υπόλοιπες. Παρακολουθούμε στενά το φαινόμενο ώστε να δούμε την εξέλιξη αλλά βλέπουμε ήδη μια τάση σταθεροποίησης της κατάστασης,γεγονός που μας κάνει να αισιοδοξούμε ότι δεν θα υπάρχουν μελλοντικά προβλήματα».
Σε κάθε περίπτωση, τογεγονός πως μετά την εφαρμογή της διαδικασίας ο ασθενής δεν έχει την ανάγκη μετάγγισης είναι άκρως σημαντικό σε ό,τι αφορά τόσο την επιτυχία της συγκεκριμένης διαδικασίας όσο και τη δυναμική της, υποστηρίζει ο καθηγητής Λεμπούλς και προσθέτει: «Πιστεύω ότι στα χρόνια που έρχονται και καθώς συνεχίζουμε να τελειοποιούμε την τεχνική,η γονιδιακή θεραπεία θα χρησιμοποιείται ευρέως για την αντιμετώπιση τόσο της θαλασσαιμίας όσο και της δρεπανοκυτταρικής αναιμίας,μιας άλλης κοινής μορφής κληρονομικής αναιμίας στην οποία εμπλέκεται επίσης το γονίδιο της β-σφαιρίνης».
Πόσος χρόνος θα απαιτηθεί για αυτή την τελειοποίηση; ρωτήσαμε τον ειδικό. «Δεν μπορώ να το προσδιορίσω χρονικά,ωστόσο πρέπει να σημειώσουμε ότι έχουν γίνει γοργά βήματα.Αν αναλογιστούμε ότι η πρώτη εφαρμογή σε ποντίκια με δρεπανοκυτταρική αναιμία έγινε πριν από μόλις δέκα χρόνια και σήμερα έχουμε έναν ασθενή στον οποίο εμφανίστηκε επιβεβαιωμένο κλινικό όφελος, όπως δείχνουν τρία χρόνια παρακολούθησης, τότε καταλαβαίνουμε ότι οι εξελίξεις τρέχουν και αναμένονται περισσότερες σύντομα».
Αν τα τρία χρόνια παρακολούθησης είναι ικανά να γράψουν τους τίτλους του… αισίου τέλους για τον ασθενή, είναι ένα εύλογο ερώτημα, το οποίο και ο ίδιος ο καθηγητής Λεμπούλς υπογραμμίζει ότι θέτει καθημερινά στον εαυτό του. «Πρέπει να συνεχιστεί η στενή παρακολούθηση του ασθενούς, ώστε να αποκλειστεί το ακόμη πιο μακροπρόθεσμο ενδεχόμενο παρενεργειών. Παράλληλα, όσο καλά και αν είναι τα δεδομένα που έχουμε αυτή τη στιγμή στα χέρια μας,δεν πρέπει να ξεχνούμε ότι αφορούν έναν μόνο ασθενή. Είναι σημαντικό να επιτύχουμε τα ίδια αποτελέσματα και σε άλλους ασθενείς». Οπως μας πληροφορεί ο καθηγητής, στις αρχές του ερχόμενου έτους η διαδικασία θα εφαρμοστεί σε έναν ακόμη ασθενή, ενώ τελικός στόχος για τη συγκεκριμένη φάση της δοκιμής είναι να περιληφθούν συνολικά 10 άτομα τόσο με θαλασσαιμία όσο και με δρεπανοκυτταρική αναιμία.
Στόχος και άλλες ασθένειες
Ο δρ Λεμπούλς τονίζει πάντως ότι η γονιδιακή θεραπεία ανοίγει τον δρόμο για την αντιμετώπιση και άλλων κληρονομικών ασθενειών. «Υπάρχουν σπάνια γενετικά σύνδρομα,τα οποία πιστεύω ότι μπορούν να αντιμετωπιστούν με γονιδιακή θεραπεία μέσω της χρήσης κυττάρων μυελού των οστών ή μέσω της λήψης τους από άλλα όργανα.Και μπορεί να είναι σπάνια, ωστόσο πλήττουν και αυτά ανθρώπους οι οποίοι αξίζουν μια καλύτερη μοίρα».
Καταλήγοντας ο καθηγητής υπενθυμίζει ότι σε πολλές περιπτώσεις οι νέες θεραπευτικές εφαρμογές εγείρουν αρχικώς αντιδράσεις προτού έλθει η επιβεβαίωση. Ενα τέτοιο επίκαιρο παράδειγμα το οποίο σχολιάστηκε κατά τη συζήτησή μας είναι εκείνο που αφορά τον καθηγητή Ρόμπερτ Εντουαρντς , τον «πατέρα» της εξωσωματικής γονιμοποίησης, ο οποίος τιμήθηκε αυτή την εβδομάδα με το Νομπέλ Ιατρικής. Μετά τη γέννηση του πρώτου «παιδιού του σωλήνα», της Λουίζ Μπράουν το 1978, υπήρξαν αντιδράσεις σχετικά με την ασφάλεια της μεθόδου και όμως σήμερα 4 εκατομμύρια παιδιά οφείλουν τη ζωή τους στη μέθοδο του βρετανού καθηγητή. «Και η γονιδιακή θεραπεία,αν μελετηθεί και εφαρμοστεί σωστά,μπορεί να χαρίσει ζωή σε πολλούς ανθρώπους» λέει ο καθηγητής Λεμπούλς. Εμείς ευχόμαστε να έχει δίκιο για το καλό εκατομμυρίων ανθρώπων. Και ίσως τότε η γονιδιακή θεραπεία της θαλασσαιμίας τιμηθεί- γιατί όχι;- ακόμη και στην αίθουσα των Νομπέλ…
ΤΙ ΕΙΝΑΙ Η ΘΑΛΑΣΣΑΙΜΙΑ
Ο όρος θαλασσαιμία ή μεσογειακή αναιμία (γνωστή παλαιότερα ως αναιμία του Cooley) αναφέρεται σε μια ομάδα γενετικών αιματολογικών διαταραχών που επηρεάζουν την παραγωγή αιμοσφαιρίνης στον οργανισμό,της πρωτεΐνης που μεταφέρει το οξυγόνο από τους πνεύμονες προς τους ιστούς και τα διάφορα όργανα του σώματος.
Η θαλασσαιμία και η δρεπανοκυτταρική αναιμία αποτελούν τις πιο κοινές κληρονομικές γενετικές ασθένειες σε παγκόσμιο επίπεδο.Εκτιμάται ότι ποσοστό της τάξεως του 5% του παγκόσμιου πληθυσμού φέρει ελαττωματικό γονίδιο της βσφαιρίνης,διαφορετικές μεταλλάξεις του οποίου προκαλούν τις δύο νόσους,ενώ περί τα 200.000 παιδιά γεννιούνται κάθε χρόνο σε ολόκληρο τον κόσμο με θαλασσαιμικό σύνδρομο.
Στην ΕΕ ένα στα 10.000 άτομα διαγιγνώσκεται με θαλασσαιμία κάθε χρόνο.
Η θαλασσαιμία εμφανίζεται σε δύο κύριες κατηγορίες: την α-θαλασσαιμία και τη β-θαλασσαιμία.Η β-θαλασσαιμία,που είναι και η πιο συχνή, «πλήττει» κυρίως τους λαούς της Μεσογείου, όπως τον ελληνικό λαό,ενώ εμφανίζεται και σε άλλες περιοχές,όπως η Νότια Ασία.Η β-θαλασσαιμία έχει τρεις μορφές,ανάλογα με την κλινική βαρύτητά της.Η μείζων β-θαλασσαιμία είναι η πλέον σοβαρή μορφή.Χαρακτηρίζεται από παντελή έλλειψη β-σφαιρίνης,προκαλώντας απειλητική για τη ζωή αναιμία,ώστε να απαιτούνται περιοδικές μεταγγίσεις αίματος εφ΄ όρου ζωής.
Τα κύρια συμπτώματα της μείζονος β-θαλασσαιμίας είναι η αναιμία,η διόγκωση του ήπατος και του σπλήνα,οι αλλοιώσεις στα οστά,η καθυστέρηση της σωματικής ανάπτυξης,αλλά και η εμφάνιση μιας παράξενης όψης του δέρματος λόγω του ίκτερου που παρουσιάζει ο ασθενής.Σήμερα η μείζων β-θαλασσαιμία αντιμετωπίζεται με μεταγγίσεις αίματος,με λήψη χηλικών παραγόντων για αποσιδήρωση (οι ασθενείς παρουσιάζουν υπερφόρτωση σιδήρου στον οργανισμό τους λόγω των συνεχών μεταγγίσεων) και πιθανώς με σπληνεκτομή.Οι χηλικοί παράγοντες λαμβάνονται υποδορίως αν και τα τελευταία χρόνια έχουν αναπτυχθεί και φάρμακα από το στόμα που χορηγούνται συνδυαστικά με την σχετικώς επώδυνη και χρονοβόρο συμβατική μέθοδο.Πολλές είναι και οι επιπλοκές της νόσου,οι οποίες εμφανίζονται σε πλήθος συστημάτων,όπως το καρδιαγγειακό και το ανοσοποιητικό,με αποτέλεσμα να απαιτούν ξεχωριστή, ανάλογα με την περίπτωση,αντιμετώπιση.
ΓΟΝΙΔΙΑΚΗ ΘΕΡΑΠΕΙΑ ΚΑΙ ΓΙΑ ΤΗ ΝΟΣΟ ΤΟΥ ΛΟΡΕΝΤΖΟ
Η ίδια θεραπευτική προσέγγιση με αυτήν που έσωσε τον νεαρό ασθενή από τη β-θαλασσαιμία είχε εφαρμοστεί προηγουμένως από ερευνητές στους οποίους συμμετείχε και ο καθηγητής Λεμπούλς για την αντιμετώπιση μιας θανατηφόρας ασθένειας του εγκεφάλου,της αδρενολευκοδυστροφίας (ΑLD).Αυτό το κληρονομικό φυλοσύνδετο νόσημα που πλήττει ένα αγόρι στα 42.000 χαρακτηρίζεται από βαθμιαίο εκφυλισμό του νευρικού συστήματος και είναι γνωστό στο πλατύ κοινό από την ταινία «Το λάδι του Λορέντζο» («Lorenzo΄s oil»).Οι ερευνητές με δημοσίευσή τους τον Νοέμβριο του 2009 στην έγκριτη επιθεώρηση «Science» ανακοίνωσαν την εφαρμογή γονιδιακής θεραπείας,και πάλι με όχημα μεταφοράς του υγιούς γονιδίου (στη συγκεκριμένη περίπτωση επρόκειτο για μη μεταλλαγμένο ΑΒCD1 γονίδιο) στα αιματικά κύτταρα τον ιό ΗΙVτου ΑΙDS σε δύο μικρούς ασθενείς ηλικίας επτά και επτάμισι ετών.Η θεραπεία έγινε το 2006 και τα παιδιά φαίνεται ότι έχουν- τουλάχιστον μέχρι στιγμής- κερδίσει το στοίχημα μιας ζωής διαφορετικής από εκείνη που είχε ο Λορέντζο.Από τότε και άλλα παιδιά έχουν ωφεληθεί από τη συγκεκριμένη σωτήρια θεραπεία.